Egy ügyeleti időben érkezett és elhunyt beteg esete a laboratóriumi szakorvos számára többféle tanulságot hordoz.
Milyen haematológiai automatát működtessünk ügyeletben?
Tudja-e értékelni az ügyeletes asszisztens a leletet?
Mit adjon át belőle a klinikusnak? Az alapparaméterektől a származtatott értékeken át az eloszlási ábrákig széles a választék. De tudja-e értékelni a klinikus, vagy ügyeljen orvos (diplomás) is?
És nézzünk magunkba. Ismeri-e eléggé minden laboratóriumi szakember a saját haematológiai automatájának lehetőségeit, értékeli-e a teljes leletet, elrendel-e, elrendelhet-e ennek alapján további vizsgálatokat?
1997. 12. 30-án 66 éves nőbeteget szállítottak a felvételes belosztályra.
1943-ban osteomyelitis
1978. uterus exst. cum adnexibus
1980. cholecystopancreatitis, cholecystectomia
1981. BHL (bilateralis hilaris lymphadenopathia) nyomán Boeck sarcoidot diagnosztizáltak
1989. ISZB, TIA, M. Hypertonicus, Boeck teljes regressio, Naprosyn allergia
3 hónap alatt kb. 10 kg-ot fogyott, gyenge-fáradékony.
Anaemia gyanú miatt háziorvosa p.o. vas therapiában részesítette.
1 hete lázas infectio, Ceclort és Mixt. pectoralist szedett.
Később már csak hőemelkedés, időnként felső hasi fájdalom.
Dyspnoe, közepes fokú icterus.
Pulmo: emphysemás
Bal rekesz felett 2 harántujjnyi tompulat
Has: hepar 2 harántujjal majus, egyenetlen felszínű
Cor: tompa, ritmusos szívhangok
EKG: Sinus ritmus, ST mérs. depr., a VL 5-6 lapos, pozitiv T-k
P: 80/min RR: 120/80 Hgmm, Anasarca nincs
A felvételt végző orvos is anaemia gyanú és feltételezett máj laesió irányában kér vizsgálatokat a laboratóriumtól, miközben a következő therapiát indítja:
|
|
2 ampulla |
Furosemid + 1 Kálium R tbl |
|
|
2 ampulla |
Histodil |
A laboratórium rövidesen bemondja a Hgb 35 20g/l, Hct 0,09, Fvs 23x109, Thrombocyta 220x109 és nagyon helyesen az MCV 125 fl haematológiai eredményeket.
Ekkor a kezelőorvos a következőket írja a kórlapba: felmerül anaemia perniciosa. A Vértranszfúziós Állomástól vércsoport meghatározást és vérválasztást kér, hogy a hypoxiás tüneteket transfusióval enyhítse.
A Hgb, Hct, MCV igen, de a fehérvérsejt és thrombocyta eredményeket alacsonynak várnánk, mivel a B12 vagy folsav hiány a DNS (purin, pirimydin bázis) synthesis zavara miatt ezen vérsejtek képzését is érinti.
A kezelőorvos visszakérdezhetett volna a vörösvérsejt egyéb származtatott értékeire is, nem tette. Az MCH-t magasnak, a MCHC-t normálnak várnánk, az RDW-CV, SD kisebb mértékű emelkedése lenne a jellemző a megaloblastos vérképzésben.
A további ügyeleti eredményekből (1. táblázat) jellemző lehet a magas LDH, de kisebb mértékű serum bilirubin emelkedés (főként indirekt - a bontást nem kérte az ügyeletes orvos) lenne jellemző.
|
1. táblázat LABORATÓRIUMI VIZSGÁLATOK
|
A rendelkezésre álló adatok alapján tehát a megaloblastos anaemia diagnózisa megingott.
Májlaesio is felmerülhetett az icterus és máj tapintási lelete alapján, de a GOT, alkalicus phos~phatase, LDH konstelláció ezt nem erősíti meg. Vizelet vizsgálat ubg, bilirubin irányában nem történt.
A Vértranszfúziós Állomás időközben jelezte, hogy a vércsoportmeghatározás sikertelen volt.
Az első mintából végzett vércsoport meghatározás eredményeket a 2. táblázat mutatja.
|
2. táblázat Az első mintából végzett vércsoport meghatározás
|
||||||||||||||||||||||||
Új mintát kértek, melyből (lásd 3. táblázat) a vércsopot megállapítható volt, O Rh (D) neg(-).
|
3. táblázat A 2. mintából végzett vércsoport meghatározás
|
||||||||||||
Hideg típusú autoimmun haemolyticus anaemia, de a kezelőorvos steroid therapiát nem indított.
Mi igazolhatta volna még ezt a feltételezett diagnózist?
A haemolysis (idő előtti sejtpusztulás) nem kompenzált, ha ilyen súlyos az anemia.
Általános leletek haemolysisben:
Az emelkedett össz bilirubinban a bontás az indirekt emelkedését bizonyítja.
Magasabb az LDH (HBDH) és a serum kálium szint. A Coombs teszt - elsősorban a direkt - pozitivitása.
Csökken a komplement felhasználás jeleként a C3 és C4, a szabad Hgb-t megkötő haptoglobin (Normál 0,5-3 g/l), ha elfogy esetleg már a hemopexin (Normál 800-1000 mg/l) is.
A serum vas decompensalt haemolysisben emelkedett, a vaskötő kapacitás csökken.
A haemolysis hideg tipusát hidegagglutinatio pozitivitás, kis(i) vagy nagy(I) elleni antitest is alátámaszthatja.
A haemolysis intra-, vagy extravasalis lehet. Az előbbit a haptoglobinhoz nem kötött Hgb-ból haemoglobinuria, illetve 6-12 óra múlva haemosiderinuria (a tubulushám sejtekben kálium ferrocianiddal kimutatott vas) igazolhatja.
Etiológiaként a beteg anamnesiséből több lehetőség felmerül, autoimmun betegség, malignitás, infectio, gyógyszerérzékenység, de ezek igazolására nem nyílt lehetőség, mert a betegnél hirtelen légzésleállás következett be, és sikertelen therapiát követően 6 és fél órás kórházi tartózkodás után beállt a halál. 5 perccel ezután jelezte a Vértranszfúziós Állomás egyetlen palack választott vér életveszély esetén történő beadhatóságát.
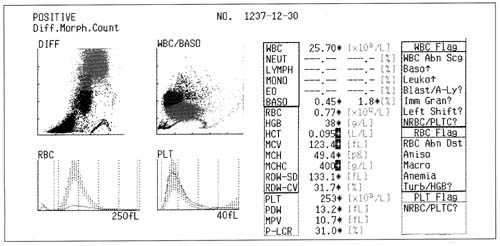
A kora reggel validáló laboratóriumi orvos a beteg sorsát nem ismerte, de látta a teljes vérkép leletet, melyet a néhány hete beállított Sysmex SF 3000-es haematológiai automatán készítettek, s amelyet a klinikus nem láthatott. Feltűnt, hogy a vörösvérsejt eloszlási görbe (histogram) formája nem látszik (1. 20ábra), csak ha kivette a referens tartomány sávját, megismételtette a mérést (2. ábra). Még jellemzőbb a Sysmex E 4000 automatán kapott lelet (3. ábra), melyen egy normál sejtpopuláció mellett egy külön macrocytaer is látható, mely miatt az MCV itt 141 lett.

1. ábra
Sysmex SF 3000 lelete.
A vörösvérsejt eloszlási görbe mögött a normál érték sáv látható

2. ábra
Sysmex SF 3000 lelete.
A vörösvérsejt hystogram mögött a referens érték sávja nincs feltüntetve.

3. ábra
Sysmex E 4000 lelete.
Összehasonlításként (4. ábra) egy valódi anaemia perniciozás lelete, a teljes vörösvérsejt populáció átlagos térfogata valóban 120-130 között van.

4. ábra
Anaemia pemiciozás lelete
Készült egy kiegészítő qualitativ vérkép és egy reticulocyta vizsgálat is.
A vérkenetben (5. ábra) a hideg típusú autoimmun haemolysisre jellemző vörösvérsejt agglutinatio mellett a haemolyticus anaemiára jellemző anisocytosis, microsphaerocytosis, polychromasia, magvas vörösvérsejtek, Jolly testek (nyilván a lép túlterhelt "pittingelő" kapacitása miatt), balra tolt vérkép, toxicus granulatio volt látható.
Szinte minden második vörösvérsejt reticulocytának (6. ábra) bizonyult (43,8 %).
|
5. ábra |
6. ábra |
Ezek a fiatal, nagy vörösvérsejtek és az autoagglutinatio hozhatta létre a haematológiai automatákban az átlagosan macrocytaernek érzékelt sejtpopulációt. A klinikus a hideg típusú autoimmun haemolyticus anaemia diagnózisát már csak a boncoláshoz leadandó adminisztrációhoz tudta használni.
A sectio a májat 1700 grammnak (normál 1500 20g), a lépet 980 grammnak (normál 150 20g) találta, szövettanilag hepatitis chronica nonspecifica, illetve hyperaemia passiva lienis és haemorrhagia lienis volt a vélemény. A közvetlen halál ok bal kamra elégtelenség; megelőző okok atheroscleroticus szívbetegség, szívizom elfajulás; alapbetegség haemolyticus anaemia. A kórbonctani és klinikai diagnózis között eltérés nem volt.
Differenciál diagnosztikailag ritka betegségként felvetődhetne még:
PNH, paroxismalis nocturnalis haemoglobinuria, mely clonalis őssejt betegség, a vörösvérsejt membran DAF (decay accelerated factor-komplement aktiválódást gátló faktor) hiánya okozza. A Ham és succrose tesztek segíthetnek a differenciálásban.
A PCH, a paroxismalis cold haemoglobinuria, igen ritka anti P antitestek által okozott, általában syphylishez társult betegség, bifázisos hideg hemolysinek in vitro kimutatásával igazolható.
A macrocytosissal járó kórképek között lehetnek még a 4. táblázatban felsoroltak.
|
4. táblázat Macrocytaer anaemiák
|
||||||||||||||
Nem, mert csak megaloblastos vérképzés esetén beszélhetünk erről. Itt reaktiv reticulocytosis (és agglutinatio) okozott egy látszólagos macrocytosist.
A gyorsan fejlődő haematológiai automatákat, leleteinek értékét a működtetőnek - s ez ma még általában a laboratóriumi orvos - jól kell ismerni (csak egy példa a referens tartomány háttérként való használata, vagy kivétele).
Lehetőleg mindent, hiszen a sok többletinformációt adó fejlesztések azért születnek, hogy a csak 1-1 esetben fontos részlelet is eljusson a klinikushoz. Természetesen a leletek felhasználásához segítséget is kell adni a felhasználóknak a készülék beállításakor.
Ha csak az alap számadatokat és flag-eket adjuk ki, ahogy ezt sokszor látjuk éppen a számítástechnikai adatátviteli hiányosságok (histogramok, scattergramok átviteli nehézsége) miatt, akkor viszont a laboratóriumi orvosnak kell szóban vagy írásban interpretálni, értelmezni az esetekben rejlő információ tartalmat a klinikus számára.
Ezek a problémák a sürgősségi osztályok beindulásával, és a kórházi intranetes hálózatok létrejöttével ismételten felmerülnek.
A válasz mindkét esetben igen.
Így, ha a napi rutinban érkezik az itt tárgyalt betegminta sürgősséggel, feltehetően 2 órán belül pontos diagnózishoz jut a klinikus, s talán a célzott therapia - az ilyenkor igen nehéz vérválasztás sikeréig is - eredményes lehetett volna.